With ferrite by TDK
GRAIN3 孤独な電子と浮かれる電子

孤独な電子と浮かれる電子
孤独な不対電子が、最外殻の軌道ではなく、そのすぐ下の順位に存在する。そのような電子配置を持つ原子の代表として、フェライト組成の骨組を成す原子番号26の鉄原子を取り上げてみよう。
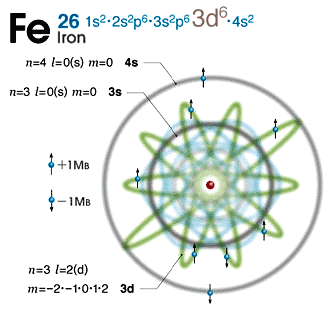
上のモデル図に示すとおり、最外殻は球対称の4s軌道であるが、なるほど正負逆のスピン磁気モーメントを持つ電子が2個納まり、定員数2を満足させている。そのすぐ内側というと、磁気量子数mが5の3d軌道、すなわち5つの軌道が重なり合うように広がる領域だが、数えてみるとそこには6個の電子しか納まっていない。モデル図左上に付した全体の電子配置を確認すると、3d軌道より内側の1sから3pまでの軌道には、許容される電子がすべて納まり、いわゆる閉殻となっている(つまり、3p軌道までの電子配置は化学的に究めて安定な希ガス原子、原子番号18のアルゴンと同じである)。となれば、3d軌道には、26-18=8個の電子が納まってもよさそうだが、なぜか、さらに2席も空席があるのに、8個のうちの2個の電子が、早々と"4階のS席"に陣取ってしまったことになる。
この勝手なふるまいの背景は、DETAIL-1に記すとして、その結果、5つの3d軌道には同じ方位を指し示す不対電子が4個も取り残され、鉄原子は磁性の均衡を大幅に崩し、電子4個分の磁性(DETAIL-2)を帯びることになる。
さて、そこでだが、4s軌道に納まった電子2個と原子核との間に働く静電的な引力、すなわち原子核と電子の結合エネルギーは極めて弱い(DETAIL-3)。つまり、ちょっとしたエネルギー(熱であるとか)を与えただけで、"特別席"の2個の電子は浮かれたように劇場(原子)の外に飛び出し、その結果として陽子2個分の正電荷を帯びた鉄イオン(Fe2+)を残すことになる。ところが、飛び出た2個の電子の方も、安定したくてうずうずしている周囲の酸素原子に引きつけられ、再び囚われの身となる。酵素原子の電子配列は、1s2・2s2・2p4だから、あと2つだけ電子を取り込めば、原子番号10の希ガス原子、ネオンと同じ電子配置のイオンとなるわけである。つまり、ひとたびは自由電子と化した2個の電子も、この酸素原子の2p軌道の2つの空席に落ち込み、今度は酸素原子を2価の負イオン(O2-)に変えてしまう。前節で予告した不対電子の"潜在能力"は、まさに、この瞬間からうごめき始めることになる。
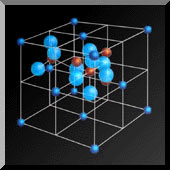
正に帯電した2価鉄と負の電荷を帯びた酸素が混在するイオン宇宙が出現すると、そこには静電気的な結合力が発生し、同種のイオンは互いに反発し、鉄イオンと酸素イオンは互いに強く引き合う。その結果、正負のイオンは交互に整然と組み合わされ、イオン宇宙は電気的に中性なイオン結晶を構築するのである。だが、その中に押し込められた鉄イオン(Fe2+)の不対電子4個分の極小磁性が、その奇怪な潜在能力を全面的に発揮するには、鉄イオン自らが、下のモデル図に示すようなイオン配置、すなわちフェライト結晶構造のかなめに陣取ることが必須の条件となる。
※DETAIL-1
これは、3d軌道と4s軌道のエネルギー準位が重なるように近接していることと、軌道の広がり、すなわち電子の存在確率の最も高いポイントを結んだ電子雲の広がりが、5つに分かれる3d軌道のひとつひとつより、4s軌道の方がはるかにゆったりとしているためである。パウリの原理により、1つの軌道には逆向きのスピンを持つ2つまでの電子しか納まることができないが、その軌道の広がりが狭ければ、-eの電荷を持つ2つの電子が出会う確率も高くなり、平均的に強い斥力(静電反発力)が発生して、その"状態"のエネルギーを高めることになるだろう。電子が存在できる軌道のポテンシャルエネルギーだけではなく、いざ電子が納まったときの状態のエネルギー上昇を考えれば、3d軌道より先に、4s軌道の方に電子が納まった方が、それだけ原子全体のエネルギーは低下することになる。1sから3p軌道までの各状態が満席となっている原子番号18の希ガス原子アルゴンのエネルギー状態は、ほかの原子と結合して分子をつくることもないほど、極めて安定しているが(ゆえに希ガス原子と呼ばれる)、その上に1個あるいは2個の電子を追加したカリウムとカルシウムが、3d軌道を無視するように、4s軌道に電子を納めるのも、以上の理由によるものと思われる。
また、このように考えると、本文中の遷移金属一覧に含まれる原子番号24のローム原子Cr、29の銅原子Cuが4s軌道に1個しか電子を持たない事情についても察することができる。つまり、3d軌道と4s軌道が重なるように隣接しているため、3d軌道に納まる電子が多くなるにつれ、4s軌道に位置する2個の電子の動きも3d軌道の電子との間に生じる斥力の増加のため制限されることになり、ひとつも電子が納まっていない3d軌道の"空部屋"に4s軌道の電子1個が引っ越した状態が、すなわちクローム原子の4s1にまつわる事情と思われる。一方、銅原子の場合は、やや単純に考えられ、4s軌道から電子が1個移れば、3d軌道は10個の電子で充填され、エネルギー的に安定な閉殻配置が完成することによる。
※DETAIL-2
電子1個に固有のスピン磁気モーメントの量子力学的磁気量は、上の原子モデルに付したように、1ボーア磁子(1MB)で表わされる。なお、ボーアという名称は、アインシュタインの唱えた光量子仮説に触発され、電子のエネルギー準位という概念を初めて原子モデルに導入した(1913年)デンマークの物理学者、ニールス・ボーアにもとづくものである。スペクトル測定から得られた磁気能率の値、
1MB=0.9274×10-23J/T(×10-21erg/G,1.165×10-29Wb・m) は、電子の軌道計算からボーアが求めた値と奇しくも一致するものであった。そのためこの名称がある。なお、一般にはボーア磁子を表わす符号としてμBが使われることが多いが、本稿では、後に登場する透磁率μと明確に区別するため、MBを採用する。
※DETAIL-3
鉄原子における原子核と電子の結合エネルギーは次のような値となる。単位は、原子物理で使われるエネルギー単位eV(1電子ボルト=1vの電位差によって1個の電子に与えられるエネルギー)である。
1s軌道:7110 2s2p軌道:827 3s3p3d軌道:95 4s軌道:7.9
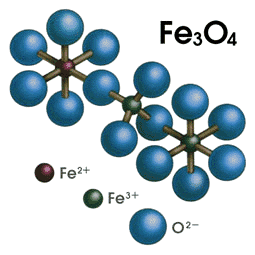
フェライト結晶構造の最小ユニットを表わしたモデル図であるが、フェライトのみならずイオン結合の結晶体は、このような最小ユニット(もちろん形態はさまざまだが)が三次元的かつ連続的につながる構造を持つ。つまり、ユニットといっても、それ自体が有限なまとまりを持つ"分子"は存在せず、イオン結晶はまさにイオン化した原子の連鎖的なつながりなのである。したがって、大きな球体で示した酸素イオンは、このユニットだけではなく隣接するユニットとも交渉を持つことになる。つまり、厳密にはこのユニットは、こうした構造を持つマグネタイトI化学式(分子式に相当する)Fe3O4を表わしていることにはならないが(正確に表わすとなると、酸素イオンの球体をこれ以外の鉄イオンと結びついている分削り取らなければならない)、視覚的な理解には大変便利なので、1化学式を構成する3個の金属イオンに注目した"部分モデル"として、これからもたびたび起用することになる。
補足
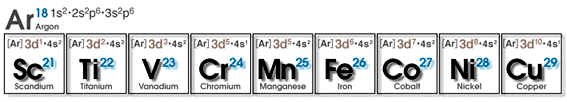
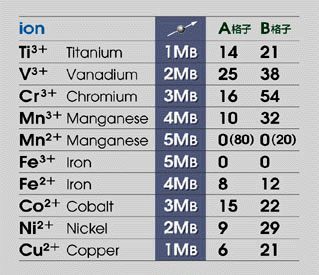
最外殻がs軌道で、その内側のd軌道の電子数が10未満であるか、10であっても最外殻に1個の電子しか納まっていない原子のことを遷移元素と呼ぶが(すべて金属なので遷移金属とも呼ばれる)、その中でも、とりわけフェライトに縁の深い1系列が上の9つの元素である。原子番号21のスカンジウムの電子配置をご覧いただくと、ほかの原子同様、3pまではアルゴンArと同じ安定した閉殻を構成し、残る3個の電子は3dに1個、4sに2個という配置になっている。3dより先に4sが充填される理由はDETAIL-1に記したが、このように3d軌道上の不対電子を割り出し、個々の原子がイオン化した際のスピン磁気モーメント量(DETAIL-2)を見たのが以下の表で、これはフェライト組成を操作する上での大変重要かつ基本的な虎の巻となる。
DETAIL-1
これは、3d軌道と4s軌道のエネルギー準位が重なるように近接していることと、軌道の広がり、すなわち電子の存在確率の最も高いポイントを結んだ電子雲の広がりが、5つに分かれる3d軌道のひとつひとつより、4s軌道の方がはるかにゆったりとしているためである。パウリの原理により、1つの軌道には逆向きのスピンを持つ2つまでの電子しか納まることができないが、その軌道の広がりが狭ければ、-eの電荷を持つ2つの電子が出会う確率も高くなり、平均的に強い斥力(静電反発力)が発生して、その"状態"のエネルギーを高めることになるだろう。電子が存在できる軌道のポテンシャルエネルギーだけではなく、いざ電子が納まったときの状態のエネルギー上昇を考えれば、3d軌道より先に、4s軌道の方に電子が納まった方が、それだけ原子全体のエネルギーは低下することになる。1sから3p軌道までの各状態が満席となっている原子番号18の希ガス原子アルゴンのエネルギー状態は、ほかの原子と結合して分子をつくることもないほど、極めて安定しているが(ゆえに希ガス原子と呼ばれる)、その上に1個あるいは2個の電子を追加したカリウムとカルシウムが、3d軌道を無視するように、4s軌道に電子を納めるのも、以上の理由によるものと思われる。 また、このように考えると、本文中の遷移金属一覧に含まれる原子番号24のローム原子Cr、29の銅原子Cuが4s軌道に1個しか電子を持たない事情についても察することができる。つまり、3d軌道と4s軌道が重なるように隣接しているため、3d軌道に納まる電子が多くなるにつれ、4s軌道に位置する2個の電子の動きも3d軌道の電子との間に生じる斥力の増加のため制限されることになり、ひとつも電子が納まっていない3d軌道の"空部屋"に4s軌道の電子1個が引っ越した状態が、すなわちクローム原子の4s1にまつわる事情と思われる。一方、銅原子の場合は、やや単純に考えられ、4s軌道から電子が1個移れば、3d軌道は10個の電子で充填され、エネルギー的に安定な閉殻配置が完成することによる。
DETAIL-2
電子1個に固有のスピン磁気モーメントの量子力学的磁気量は、上の原子モデルに付したように、1ボーア磁子(1MB)で表わされる。なお、ボーアという名称は、アインシュタインの唱えた光量子仮説に触発され、電子のエネルギー準位という概念を初めて原子モデルに導入した(1913年)デンマークの物理学者、ニールス・ボーアにもとづくものである。スペクトル測定から得られた磁気能率の値、 1MB=0.9274×10-23J/T(×10-21erg/G,1.165×10-29Wb・m) は、電子の軌道計算からボーアが求めた値と奇しくも一致するものであった。そのためこの名称がある。なお、一般にはボーア磁子を表わす符号としてμBが使われることが多いが、本稿では、後に登場する透磁率μと明確に区別するため、MBを採用する。

TDKは磁性技術で世界をリードする総合電子部品メーカーです